来源:小编 更新:2024-10-23 03:03:35
用手机看
电荷平衡,又称为电中性规则,是化学溶液中一个基本且重要的概念。它指的是在溶液化学平衡体系中,各种荷电型体所荷单位正电荷的总浓度必须等于所荷单位负电荷的总浓度。这一规律确保了溶液总是电中性的,对于理解溶液中的化学反应和离子行为具有重要意义。
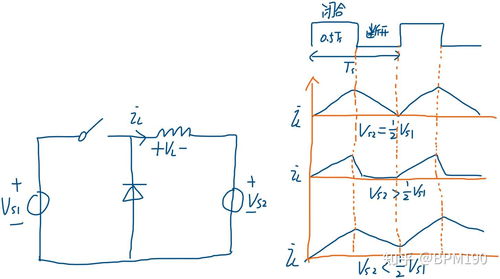
电荷平衡的原理基于溶液的电中性原则。在溶液中,正离子和负离子通过静电作用相互吸引,形成稳定的离子对。为了保持溶液的电中性,溶液中正离子的总电荷量必须与负离子的总电荷量相等。这一原则在所有电解质溶液中都适用,无论是强电解质还是弱电解质。

在化学领域,电荷平衡可以帮助我们理解溶液中的离子反应,预测反应的产物和反应速率。
在生物学领域,电荷平衡对于维持细胞内外的离子平衡至关重要,这对于细胞的生命活动至关重要。
在环境科学领域,电荷平衡可以帮助我们评估水体中的污染程度,以及污染物在水体中的迁移和转化过程。
在计算电荷平衡时,我们需要考虑溶液中所有离子的电荷和浓度。以下是一个简单的电荷平衡计算示例:
假设有一个溶液,其中包含以下离子:Na+、Cl-、NO3-、K+和SO42-。我们需要计算溶液中的电荷平衡。
首先,列出所有离子的电荷和浓度:
离子
电荷
浓度
Na+
+1
0.1 M
Cl-
-1
0.2 M
NO3-
-1
0.1 M
K+
+1
0.2 M
SO42-
-2
0.1 M
接下来,计算正负电荷的总和:
正电荷总和 = 0.1 M × (+1) + 0.2 M × (+1) = 0.3 M
负电荷总和 = 0.2 M × (-1) + 0.1 M × (-1) + 0.1 M × (-2) = -0.4 M
由于正负电荷总和不相等,我们需要调整溶液中的离子浓度,以使电荷平衡。例如,我们可以通过添加或移除离子来调整浓度,直到正负电荷总和相等。
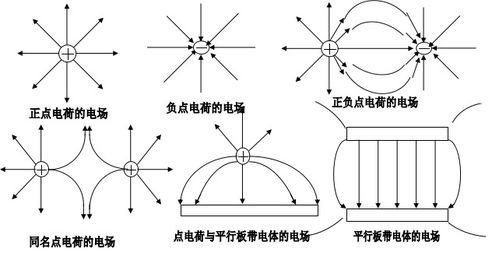
在处理电荷平衡问题时,需要注意以下几点:
确保所有离子的电荷和浓度都已正确计算。
考虑溶液中的离子强度和离子间的相互作用。
注意溶液的酸碱性质,因为酸碱反应会影响电荷平衡。
电荷平衡是化学溶液中的一个基本概念,对于理解溶液中的化学反应和离子行为具有重要意义。通过掌握电荷平衡的计算方法和注意事项,我们可以更好地理解溶液中的化学现象,并在实际应用中取得更好的效果。